中心调研是对研究者和研究中心是否有能力承接项目进行初步的评估。对研究者的资质、专业性、合作意愿、临床试验经验等各方面进行筛选和评定。这一点对于临床试验在该中心的开展至关重要。做好可行性研究,也是给项目组提供了是否在该中心开展研究的依据。同时也可以对将来可能会遇见的问题,有个提前的预判。
申办方选择中心的重要指标往往是启动快、入组快、质量高、费用低,所以在调研阶段,需要考察以下几点:
- 医院的资质是否符合要求
- 机构流程是否清晰规范,有明确的规章制度
- 研究者资质是否符合要求
- 科室的影响力、声誉、病源情况,是否能及时招募到足够受试者
- 科室竞争项目情况
- 中心的既往项目质量是否可靠
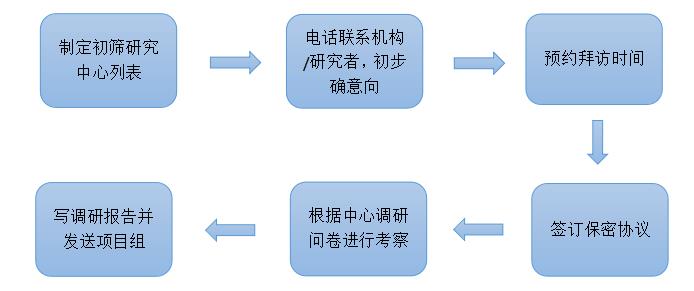
1.初步筛选研究中心,确认调研列表
中心调研阶段的调研列表有多个来源:主要研究者推荐、CRO推荐、既往合作过不错的中心、根据医院备案资质进行符合条件的筛选等。根据初步确认的中心制定调研列表。
医院的资质是指医院乃至具体科室是否开展临床试验的资质,在预筛中心时我们做的第一件事情就是查看目标中心及目标项目组是否具备开展临床试验的资质。这些资质的查询可以通过“药物和医疗器械临床试验机构备案管理系统”,地址为:https://beian.cfdi.org.cn/CTMDS/apps/pub/public.jsp
查询完资质,下一步便是收集机构和伦理的相关信息,可以通过医院官网,也可以通过驭时临床试验、药研社等一系列公众号或APP获取目标中心的机构伦理的邮箱及联系电话。
2.中心调研
一般的步骤是先与机构联系,由机构联系PI。当然也不排除申办方与PI相熟,或者有过合作经验,先行找PI沟通确认再找机构的情况。
初次电话联系研究者时,可以参考这个模板:
“XX老师/主任您好,我是XXX公司的XXX,我们有个XXX的临床试验,想要在你们医院/科室展开,不知道您这边有没有兴趣承接?”
“项目是XXX类的,国际多中心/国内的,组长单位XXX,总共入XX病人,计划在本院入xx例,主要是要XXX的病人,XXX使用方法、作用机理、优势等”(抓住重点,尽量简洁明确)
如果机构和主任都确定有意向承接项目之后,可以和主任预约时间到科室进行调研。
一般有承接过临床试验的中心科室会知道调研的目的,主任可能会指派一位科室管理GCP的秘书或者SUB-I负责对接,可以按照需要了解的情况进行调研。
完善的可行性调研包含许多内容,如中心的认证专业、立项流程、伦理上会频次及流程、研究合同签署流程、医院影响力、研究者合作基础,既往临床试验质量、成本、中心的入组潜力、入组能力、是否有CRC需求等。如果公司有其他需要调研的信息列表,也可一并咨询。
如果调研时间充裕、条件允许的话,也可以一同拜访一下机构和伦理,了解一下具体流程,留一下联系方式。
3.调研报告
完成调研后,及时填写中心调研报告并提交项目组,最终由项目组确定合适的研究中心。
相关往期文章:
