随着新型冠状病毒肺炎疫情逐渐得到控制,各省份的医疗器械应急审批通道纷纷关闭。很多企业通过应急审批通道,顺利拿到了防护类产品的应急审批注册证。然而还有很多企业则错过了应急审批期,仍然想去申报注册医用口罩、防护服等产品,此种情况下该如何申报,本文就此问题进行了回答,整理了医用口罩、防护服等防护产品的注册申报流程。
一、医用口罩、防护服注册审批流程图
医用口罩和防护服均为第二类医疗器械,需要向各省份的药品监督管理局进行注册申报。
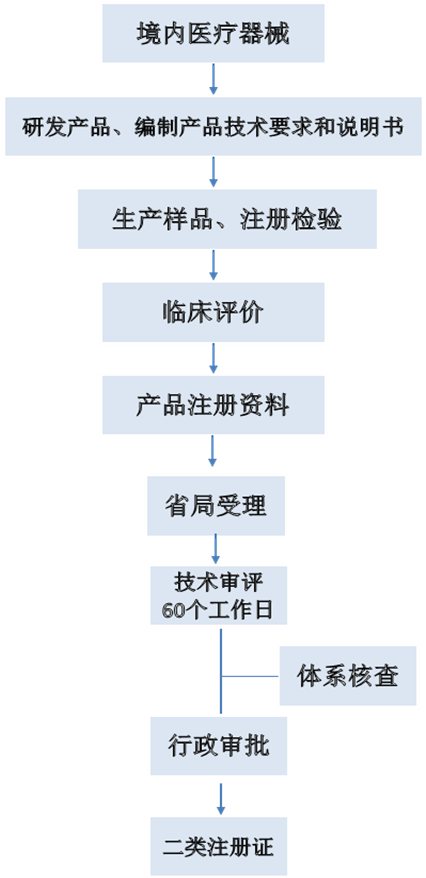
二、医用口罩、防护服注册申报资料
每个省份对第二类医疗器械注册申报的资料要求略有不同,企业应以各省份发布的相关政策为准,本文以浙江省为例,介绍口罩、防护服在申报注册时应提交哪些资料。
序号 | 注册资料 | |
1 | 申请表 | |
2 | 证明性文件 | |
3 | 医疗器械安全有效基本要求清单 | |
4 | 综述资料 | 概述 |
产品描述 | ||
型号规格 | ||
包装说明 | ||
适用范围和禁忌症 | ||
参考的同类产品或前代产品 | ||
其他需说明的内容 | ||
5 | 研究资料 | 产品性能研究 |
生物相容性评价研究 | ||
生物安全性研究 | ||
灭菌/消毒工艺研究(无菌产品) | ||
产品有效期和包装研究 | ||
其他资料 | ||
6 | 生产制造信息 | 生产加工工艺 |
生产场地信息 | ||
7 | 临床评价资料 | |
8 | 产品风险分析资料 | 风险分析 |
风险评价 | ||
风险控制措施的实施和验证 | ||
任何一个或多个剩余风险的可接受性评定 | ||
9 | 产品技术要求 | |
10 | 产品注册检验报告 | 注册检验报告 |
预评价意见 | ||
11 | 产品说明书和最小销售单元标签样稿 | |
12 | 符合性声明 | |
三、医用口罩的相关注册信息
1.分类
医用口罩分为医用防护口罩、医用外科口罩、一次性使用医用口罩。
2.产品描述
医用防护口罩:由一种或多种对病毒气溶胶、含病毒液体等具有隔离作用的面料加工而成的口罩。在呼吸气流下仍对病毒气溶胶、含病毒液体等具有屏障作用,且摘下时,口罩的外表面不与人体接触。
医用外科口罩:通常由面罩、定形件、束带等组件加工而成,一般由非织造布材料制造而成。通过过滤起到隔离作用。
一次性使用医用口罩:通常采用无纺布或无纺布复合材料制成,可为二层或三层结构,可有可塑性鼻夹,口罩带为弹性或非弹性,具有过滤颗粒物和细菌等特性。
3.预期用途
医用防护口罩:戴在医疗机构与病毒物料接触的人员面部,用于防止来自患者的病毒向医务人员传播。
医用外科口罩:用于戴在手术室医务人员口鼻部位,以防止皮屑、呼吸道微生物传播到开放的手术创面,并阻止手术病人的体液向医务人员传播,起到双向生物防护的作用。
一次性使用医用口罩:用于临床各类人员在非有创操作过程中佩带,覆盖住使用者的口、鼻及下颌,为防止病原体微生物、颗粒物等的直接透过提供一定的物理屏障。
4.技术指标
医用防护口罩:依据GB 19083-2010 医用防护口罩技术要求。
医用外科口罩:依据YY 0469-2011 医用外科口罩。
一次性使用医用口罩:依据YY/T 0969-2013 一次性使用医用口罩。
5.可参考的指导原则
医用口罩产品注册技术审查指导原则(2014年第7号)
链接:https://www.cmde.org.cn/CL0112/6134.html
四、防护服的相关技术信息
1.产品描述
由一种或多种对病毒气溶胶、含病毒液体等具有隔离作用的面料加工而成的衣服。脱下时,防护衣的外表面不与人体接触。
2.预期用途
用于医疗机构医护人员穿的职业防护衣。阻止来自患者的病毒随空气或液体向医务人员传播。
3.技术指标
防护服:依据GB 19082-2009 医用一次性防护服技术要求。
