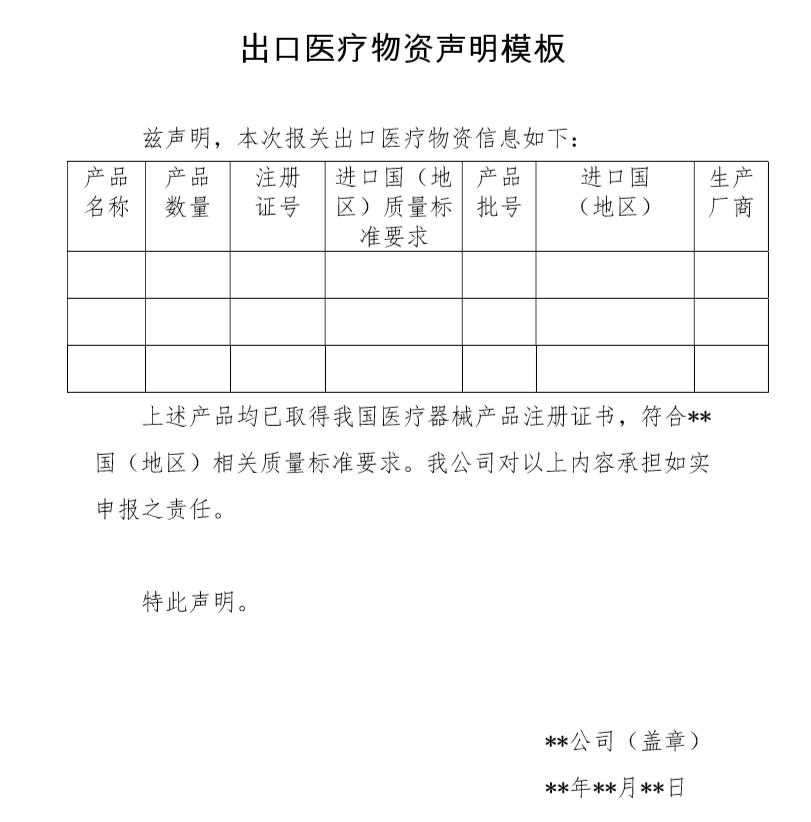
近日,各国媒体报道中国出口的口罩、试剂等防疫医疗物质存在质量问题,在疫情防控特殊时期,为有效支持全球抗击疫情,保证产品质量安全、规范出口秩序,国家商务部、海关总署和国家药品监督管理局联合发布关于有序开展医疗物质出口的公告(2020年第5号),公告要求自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计等医疗物质的企业出口报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求,海关凭药品监督管理部门批准的医疗器械产品注册证书放行。
依据该公告,未获得国内注册证的医疗器械不得出口,药监部门不再出具《医疗器械产品出口销售证明》,海关也不放行。因此在当前形势下,医疗器械企业应首先获得国内药监批准的医疗器械注册证和医疗器械生产许可证,才能正常的出口。
瑞旭集团提醒医疗器械企业,特别是一些“民转医”或跨界进入的企业,医疗器械生产销售应按照医疗器械法规要求,规范生产质量管理体系,通过产品安全性和有效性验证,向药监部门申办医疗器械注册证和生产许可证。而作为防疫医疗物质基本是按照II类或III类医疗器械管理,其注册申报和体系要求都比较高,建议企业提前准备注册申报,以免出口受阻,内销又不合规。