近期药械圈搜索词排行榜占首位的一定是应急审批,但随着疫情的好转,各地药品监督管理部门都陆续发布关于停止应急审批申请有关事项的通告。例如:江苏省3月22日发通知:停止受理医用防护服医用口罩应急审批申报申请有关事项。
随着应急审批通关的关闭,针对应急审批的医疗器械注册证到期后,部分省将优先纳入到优先审批通道,与应急审批相似,医疗器械优先审批同样在注册申请、技术审评、行政审查等环节优先安排,能给生产企业注册申报医疗器械带来不少的便利。
优先审批的优势:
1. 审批优先排队
器审中心对列入优先审批的医疗器械注册申请,按照接收时间单独排序,优先进行技术审评。
2. 体系核查优先
对于优先审批的项目,省级食品药品监督管理部门优先安排医疗器械注册质量管理体系核查。
3. 审批优先
对于优先审批的项目,器审中心在技术审评报告中注明为优先审批项目,国家食品药品监督管理总局优先进行行政审批。
4. 专项交流
对于优先审批的项目,器审中心在技术审评过程中,应当按照相关规定积极与申请人进行沟通交流,必要时,可以安排专项交流。
5. 优先审批过程分同步确定
对于申请优先审批的境内医疗器械注册申请项目,器审中心确认该产品属于第二类医疗器械的,受理部门及时将第二类医疗器械注册申报资料和分类意见转申请人所在地省级食品药品监督管理部门审评审批。
这些优势促使产品整个注册上市周期提前,为企业迎得了上市的时间,抢占市场先机。
申请优先审批的条件:
国家食品药品监督管理总局对符合下列条件之一的境内第三类和进口第二类、第三类医疗器械注册申请实施优先审批:
(一)符合下列情形之一的医疗器械:
1.诊断或者治疗罕见病,且具有明显临床优势;
2.诊断或者治疗恶性肿瘤,且具有明显临床优势;
3.诊断或者治疗老年人特有和多发疾病,且目前尚无有效诊断或者治疗手段;
4.专用于儿童,且具有明显临床优势;
5.临床急需,且在我国尚无同品种产品获准注册的医疗器械。
(二)列入国家科技重大专项或者国家重点研发计划的医疗器械。
(三)其他应当优先审批的医疗器械。
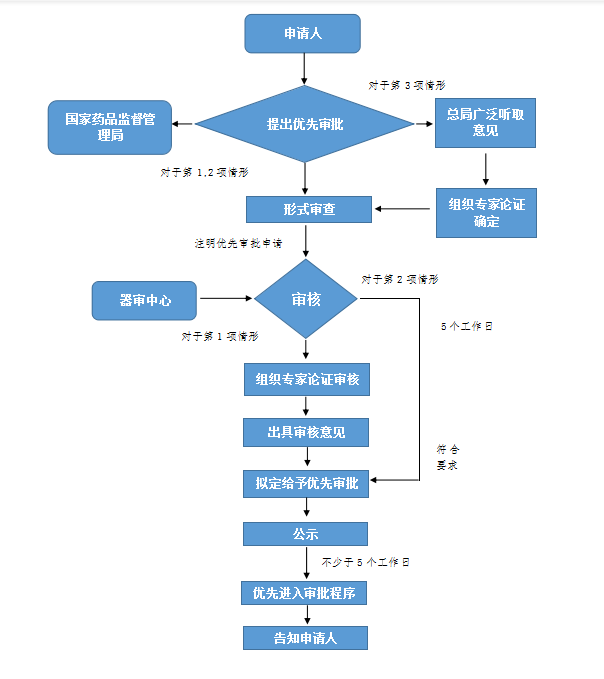
优先审批的流程及要求: