我国是世界上较早制定新食品原料(旧称新资源食品)管理制度的国家。1983年的《食品卫生法》(试行)中首次提出了利用新资源生产的食品必须经卫生部门审批,原卫生部于1987年发布首个配套法规。经过30多年的发展,众多新食品原料获得批准,并广泛应用于各类食品中。
1. 新食品原料的发展历程
从1987年至今,新食品原料的审批历经了四部法规的变迁,管理方式发生了很大的变化,法规监管体系日益完善。
表1 新食品原料的政策发展历程
时间段 | 法规 | 历史名称 | 管理对象 | 主要管理方式及变化 |
1987-1990 | 《食品新资源卫生管理办法》 | 新资源食品 | 终产品或食品原料 | 由于年代久远,该阶段的管理办法原文已无官方公告可寻。 |
1990.07.27-2007.11.30 | 《新资源食品卫生管理办法》 | 新资源食品 | 终产品或食品原料 | I. 该阶段的产品在获准正式生产前必须经过两年试生产阶段,而后方能申请正式生产批件; II. 审批通过后向该产品的申报企业核发批准证书; |
2007.12.01-2013.09.30 | 《新资源食品管理办法》 | 新资源食品 | 食品原料 | I. 取消了试生产制度; II. 管理对象变为“食品原料”; III. 由“单个终端产品发证”转变为“以名单形式向社会公告”, 避免了同类产品的重复审批; IV. 提出了“实质等同”审查制度。 |
2013.10.01-至今 | 《新食品原料安全性审查管理办法》 | 新食品原料 | 食品原料 | I. “新资源食品”正式被“新食品原料”取代,并重新定义了新食品原料的范围; II. 申报资料中增加了由风险评估单位出具安全性评估意见的要求; III. 增加了向社会征求意见的审核程序。 |
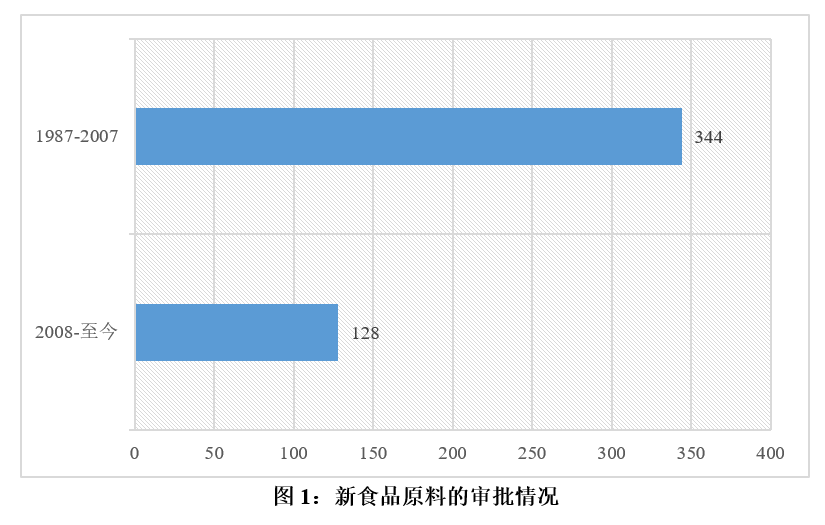
据统计,1987-2007年的20年间,原卫生部共计批准了344个新资源食品,其中大量产品以终产品形式获得批准,例如天府可乐、少林可乐、中国花粉口服液等。而经过2年的试生产后申请转为正式生产的产品仅有76个,占全部批准总数的22%。
2007年12月1日起,我国新食品原料的管理理念发生变化,审批对象转为食品原料。2008年至今,共计128个新食品原料获得批准,其中原料新品种和微生物新品种分别为105个和23个。您可通过获取瑞旭集团发布的《新食品原料中国市场准入指南》查看详细的批准名单。
2. 新食品原料的应用
新食品原料源于食品工业日新月异的发展。将新食品原料应用于食品生产中,亦是企业自我创新,开拓新市场的手段之一。自我国新食品原料以食品原料为审评对象批准以来,一系列获得批准的新食品原料得以在各类食品中发光发热。
2.1 在普通食品中的应用
新食品原料在普通食品中的应用十分广泛,鱼油凝胶糖果、玛咖固体饮料、蓝莓叶黄素酯压片糖果、芦荟含乳饮料(库拉索芦荟凝胶)等各类产品中均涌现出了新食品原料的身影。预包装普通食品企业在使用某种新食品原料时,应严格按照批准公告执行,尤其需注意以下三方面:
- 使用范围
- 食用量
- 标签、说明书要求
表2 新食品原料应用于普通食品中的注意事项
举例 | 公告相关内容 | 注意事项 |
乳木果油 | 使用范围:巧克力、糖果、冰激淋、烘焙产品及煎炸油,但不包括婴幼儿食品。 | 仅公告所列的几个产品类别可使用乳木果油,其他食品类别(如饮料)等均不可添加乳木果油。 |
玛咖粉 | 1)食用量≤25克/天; 2)婴幼儿、哺乳期妇女、孕妇不宜食用;食品的标签、说明书中应当标注不适宜人群和食用限量。 | I. 根据产品的净含量、食用方法等情况适当添加玛咖粉; II. 应在产品标签上标识如下信息: 本品含xx克玛咖粉。玛咖粉食用量应≤25克/天,且婴幼儿、哺乳期妇女、孕妇不宜食用。 |
2.2 在保健食品中的应用
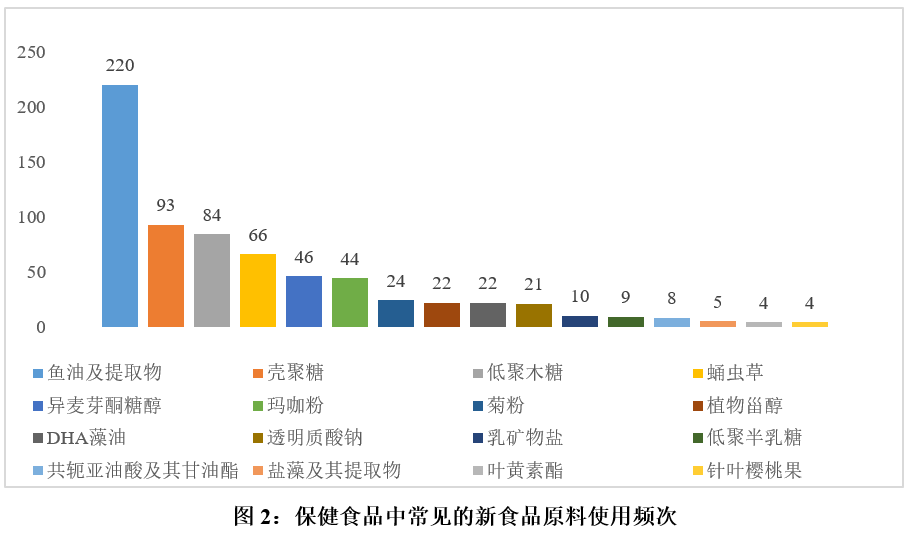
已批准的新食品原料可作为保健食品的原料来源之一。据瑞旭集团的统计,已注册保健食品中常见的新食品原料使用情况如图2所示(实际上,鱼油、壳聚糖这些应用频次较高的原料,在被批准为新食品原料前,在保健食品中已有一定的使用历史)。从这些应用中也可以看出,脂类原料和碳水化合物类原料是在保健食品中最受欢迎的两大新食品原料。
除此之外,酵母β-葡聚糖、珠肽粉、γ-氨基丁酸、杜仲籽油、短梗五加等已批准的新食品原料也均在保健食品中有少量应用。
值得一提的是:在保健食品中使用新食品原料时,保健食品企业通常会向获得国家卫建委(原卫计委、原卫生部)新食品原料批准的厂家购买原料,并索取相关的批准文件,以避免在保健食品注册申报过程中,证明所使用的原料与批准的原料具有实质等同性的过程。
2.3 在特殊医学用途配方食品中的应用
特殊医学用途配方食品(FSMP)中添加新食品原料,应当按照批准公告的要求执行,同时满足FSMP的食品安全国家标准及相关规定。
例:某COPD病人用全营养配方食品中添加鱼油及提取物,需注意:
I. 鱼油及提取物的成分和质量要求等符合原卫生部2009年第18号公告的规定;
II. 产品中鱼油及提取物的含量需按照GB29922问答中,对于n-3脂肪酸(以EPA和DHA)的含量规定进行适当调整。
目前,FMSP中新食品原料的应用并不广泛。FSMP注重产品对进食受限或特定疾病状态下人群的营养补充与支持作用,而许多新食品原料,由于其对营养补充、支持所起到的作用非常有限或是含有FSMP中不允许添加的其他生物活性成分,因而并不适用于FSMP。企业在选用某种新食品原料时,应当首先考虑此物质加入配方后起了哪些方面的营养支持、补充的作用。
(PS. 更多关于FSMP中原料的使用,您可点击特殊医学用途配方食品原料浅析进行查看)
3. 未来,哪些新食品原料在路上
目前,根据国家食品安全风险评估中心的相关公告,赶黄草、β-1,3-葡聚糖、瑞士乳杆菌R0052、婴儿双歧杆菌R0033、两歧双歧杆菌R0071……等申报的新食品原料都已对外公开征求意见。若它们都能顺利通过最终审批,食品企业们将获得更广阔的原料选择空间,让我们共同期待!
我们的服务:
