2019年以来,国家市场监督管理总局陆续发布了一系列有关保健食品的政策法规,大力推进保健食品注册与备案双轨制运行,进一步明确保健食品的管理要求,填补相关政策文件空白。瑞旭集团带您了解这些法规文件所释放的信号。
- 2019年发布的相关法规文件
项目 | 法规文件 | 实施/发布日期 |
正式稿 | 《保健食品原料目录与保健功能目录管理办法》 | 2019.10.01实施 |
2020.01.01实施 | ||
征求意见稿 | 2019.03.20发布 | |
2019.04.01发布 | ||
2019.04.08发布 | ||
2019.04.08发布 | ||
2019.06.04发布 | ||
《保健食品卫生学理化检验规范(征求意见稿)》 | 2019.06.19发布 | |
《特殊食品注册现场核查工作规程(暂行)(征求意见稿)》 | 2019.07.17发布 |
- 备案目录有望进一步扩大
2019年4月1日,市场监管总局发布了辅酶Q10、褪黑素、鱼油、破壁灵芝孢子粉和螺旋藻5种保健食品原料目录的征求意见稿,相关保健功能涉及增强免疫力、抗氧化、辅助降血脂和改善睡眠。紧随其后,备案可用辅料发布增补名单并向公众征求意见,拟新增包括大豆磷脂、姜黄素、果蔬粉、低聚果糖等在内的17个辅料。
这是继保健食品备案制度实施以来,市场监管总局首次发布非“补充维生素矿物质”类备案原料的征求意见稿,预示着我国进一步扩大保健食品备案目录,从而激发市场活力,减轻企业负担的步伐向前迈进了一大步。预计随着保健食品原料目录的扩大,未来备案产品将会成为主要趋势。
- 保健食品注册审批速率快速提升
自《保健食品注册与备案管理办法》实施以来,注册类产品的审批一度陷入了停滞状态。虽然2017年有数百款产品拿到注册证,但均为备案制度实施前获批的营养素补充剂,无一款功能性产品获批。而2018年全年仅批准了10款注册产品。究其原因,保健食品注册新旧政策交替和国家机构改革是两个关键。
自2019以来,注册类产品的批准速率已显著提升。截至2019年9月25日,涉及新产品注册、延续注册、变更注册、转让技术四方面共计640款产品获得批准,详见下图。
其中,全年合计已有153款保健食品获得新产品注册批件(请点击“2019年保健食品注册数据分析”了解详情)。此外,延续注册批准公告更是络绎不绝,目前已有414款产品获批。总体看来,我国保健食品注册审批工作已在稳步开展中,此前积压的产品正在得以解决,相信陆续会有更多的产品获得批准。
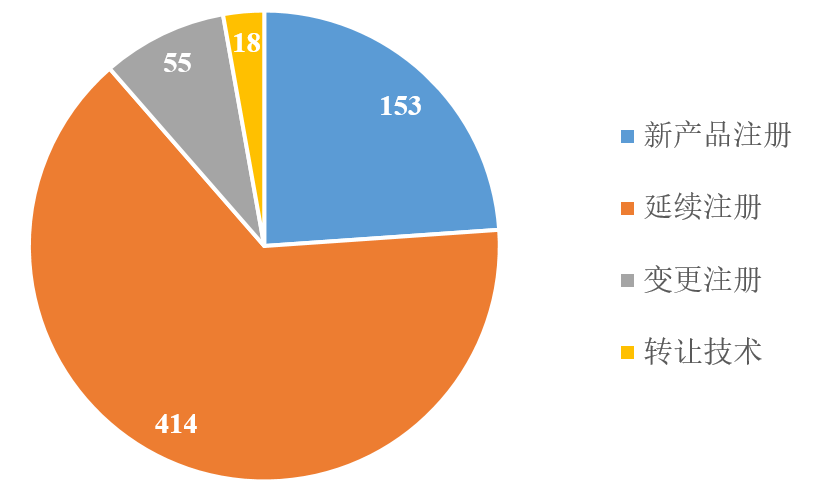
图1 2019年我国保健食品注册批准情况(个数)
- 注册产品检测方法陆续发布草案
2018年7月,《保健食品检验与评价技术规范(2003版)》被废止后,众多企业暂停了新产品的注册检验工作。无检测依据,新品注册工作无法推进,使得新检测方法的发布成为了万众期待之事。
为加强保健食品检验与评价技术工作的管理,市场监管总局组织启动了对《保健食品检验与评价技术规范》的全面修订工作,2019年已陆续发布:《保健食品毒理学评价程序》、《保健食品用菌种致病性评价程序》及《保健食品卫生学理化检验规范》三个征求意见稿。
我们相信,在此之后,功能评价方法的征求意见稿也将很快发布。据了解,为解决目前无功能评价依据的问题,《保健食品检验与评价技术规范(2003版)》与2012年修订的9个保健功能评价方法将可能被合并为一个新版本尽快发布,其中功能评价方法不做重大改变,待后续再对评价方法进行深入修订。相关信息仍以最终发布的版本为准,让我们共同期待功能评价方法的早日发布!
- 任何单位或个人可对原料目录或功能目录提出建议
2019年10月1日,《保健食品原料目录与保健功能目录管理办法》将正式实施。该办法规定,任何单位或个人在科学研究论证的基础上,均可提出纳入保健食品原料目录和功能目录的建议。主管部门按程序要求组织审查、公开论证,符合要求的就可以纳入目录。
这一管理办法的发布是史无前例的,具有里程碑意义。它打通了新的备案原料和新的保健功能的研究开发路径,鼓励企业研发与创新,可以充分发挥社会资源科研优势,从而促进保健食品行业的高质量发展。
结语
今年以来,保健食品新政策不断发布,产品审评速率加快,利好行业发展。当然,在注册类产品有望向前迈进之时,企业在准备申报卷宗之时,需注重产品的研发过程,强调配方的科学性,并具有充分的科学依据支持。
另一方面,市场监管总局仍在大力加强对保健食品行业虚假宣传的严格监管,同时强化标签标识要求,如2020年1月1日起保健食品标签需标注警示语。这些举措也有利于强化企业主体责任,体现对消费者负责的态度,同时有利于保护消费者知情权,让消费选择更加理性,利于行业的长期发展。
作者:于艳艳
